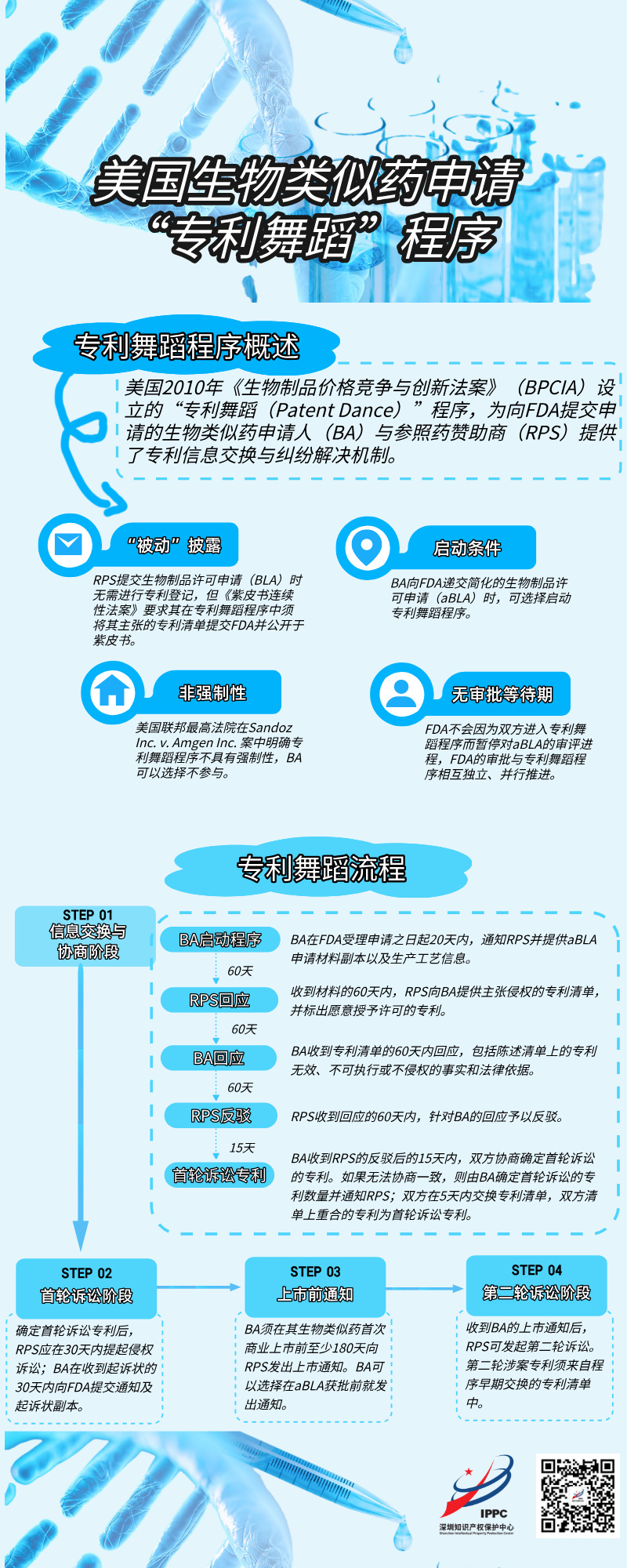
近年来,中国生物医药企业出海步伐加快,本土研发药品在海外市场获批或进入审评阶段的数量持续增加。美国作为全球最大的生物医药消费市场,对中国药企实现全球化布局具有重要战略意义。生物医药领域素来是专利纠纷的高发地带,例如仿制药与生物类似药在上市过程中常遭遇原研药企的专利阻击,专利纠纷因而成为影响产品商业化进程的关键变量。为了平衡商业利益和鼓励创新,美国法律设计了一系列争议解决机制,例如2010年《生物制品价格竞争与创新法案》(Biologics Price Competition and Innovation Act,下称“BPCIA”)设立的“专利舞蹈(Patent Dance)”程序。该程序为向美国食品药品监督管理局(FDA)提交上市申请的生物类似药申请人(Biosimilar Applicant,下称“BA”)与参照药赞助商(Reference Product Sponsor,下称“RPS”,即生物制品原研厂商)提供了专利信息交换与纠纷解决机制,熟悉该程序有助于企业更好地应对专利风险、调整产品上市计划。本报告将围绕该程序的法律依据、启动条件及核心流程等展开分析,供有关部门及企业参考。
一、专利舞蹈程序概述
生物制品是指来源于生物体或通过生物工程技术制备的复杂混合物或生物大分子,例如疫苗、重组蛋白类药物、核酸类药物、细胞治疗类药物等。生物类似药则是指在质量、安全性和有效性方面与已获批的参照药具有相似性的生物制品。
生物制品由于结构复杂、生产工艺特异,使得生物类似药虽可达到与参照药高度相似,却难以实现完全一致。这与原研化学药及其仿制药的情况不同,化学药的活性成分通常由结构明确、可完全复制的纯化学物质组成,因此仿制药一般含有与原研化学药完全相同的活性成分。上述仿制药与生物类似药的本质差异,决定了两者在专利纠纷解决机制方面存在不同。为了更好地陈述生物类似药相关的专利舞蹈程序,下文将会提及1984年Hatch-Waxman法案所确立的与仿制药相关的专利链接制度的部分内容。
(一)“被动”披露
Hatch-Waxman法案要求原研药企在向FDA进行新药上市申请时,必须主动登记该药品活性成分、制剂/组合物、使用方法相关的专利信息于“橘皮书(Orange book)”(即《经过治疗等效性评价批准的药品》)。基于这种信息的透明性,仿制药企向FDA提交简化新药申请时,必须对照橘皮书中登记的原研药专利,提交以下四类声明之一:第I类声明是橙皮书无相关专利信息;第II类声明是橙皮书所列专利已过期;第III类声明是所列专利即将过期,承诺在专利过期后才上市;第IV类声明是所列专利无效或其仿制药不侵权。针对IV类声明,原研药企可在收到通知后的45天内提起专利侵权诉讼。
对于生物制品,虽然存在“紫皮书 (Purple Book)”(即《具有参照药独占权及生物类似性/可互换性评价的获许可生物制品清单》),但RPS没有义务主动在紫皮书上进行专利登记。在《紫皮书连续性法案》(The Purple Book Continuity Act)2021年生效后,RPS才被要求须在专利舞蹈过程中,将其主张可能被侵权的专利清单提交FDA并公开于紫皮书。也就是说,紫皮书的披露是“被动”且具有滞后性的,BA无法像仿制药申请人那样事先获知原研生物制品相关的专利信息,而只能通过专利舞蹈过程中的信息交换环节,才得以知晓。
(二)启动条件
生物制品在美国申请上市时须向FDA提交生物制品许可申请(Biologics License Application, BLA),申请者通常需提交全套完整的研究资料,以证明产品的安全性、纯度和效价。针对生物类似药,BPCIA设立了简化的生物制品许可申请(abbreviated Biologics License Application, aBLA)途径。在此途径下,BA可依赖RPS已获批的数据,其所需的临床研究资料得以大幅简化。BPCIA规定,RPS在其原研生物制品获得FDA批准上市之日起,将获得12年的市场独占期。这期间FDA不得批准相应生物类似药上市,并且在独占期的前4年,FDA不得受理BA提交的aBLA。在上述4年的窗口期之后,当BA向FDA递交aBLA时,可选择启动专利舞蹈程序。
(三)非强制性
美国联邦最高法院在2017年Sandoz Inc. v. Amgen Inc. 案中明确,专利舞蹈程序不具有强制性,BA可以选择不参与。但若BA选择不参与专利舞蹈,RPS就可立即基于任何相关专利提起诉讼,无需经过繁琐的信息交换和协商过程。这不仅可能导致诉讼时间提前,并且涉诉专利的选择权完全掌握在RPS手中。
(四)无审批等待期
对于仿制药,Hatch-Waxman法案规定仿制药申请人作出第IV类声明后,若原研药企在45天内提起诉讼,FDA将自动暂停仿制药的上市审批,进入最长30个月的审批等待期。而对于生物类似药,FDA并不会因为双方进入专利舞蹈程序而暂停对aBLA的审评进程。换言之,FDA的审批与专利舞蹈程序相互独立、并行推进。
二、专利舞蹈程序流程
美国专利舞蹈程序的具体流程主要包括以下阶段:
(一)信息交换与协商阶段
1.BA启动专利舞蹈程序
若选择参与专利舞蹈程序,BA应在aBLA获得FDA受理之日起20天内,通知RPS并提供以下材料:(1)aBLA申请材料副本以及相关生物仿制药的生产工艺信息;(2)RPS合理要求的其他额外信息。上述材料有助于RPS了解生物类似药在研发与生产过程中所涉及的具体技术,从而判断哪些专利可能被侵权。这也意味着,BA的高度敏感信息将直接向其市场竞争对手披露,因此避免敏感信息暴露也是部分BA选择不参与专利舞蹈程序的重要考量因素之一。
2.RPS回应
RPS在收到上述材料后的60天内,需向BA提供一份可合理主张专利侵权的专利清单(下称“A专利清单”),并标出其愿意向BA授予许可的专利。
3.BA回应
BA在收到上述专利清单后,需要在60天内予以回应:(1)需向RPS提供详细陈述,针对清单上专利权利要求逐项地说明认为专利无效、不可执行或不侵权的事实和法律依据;或提供专利权到期前不上市的声明。(2)亦可向RPS提供一份BA认为的RPS可合理主张侵权的额外专利清单(下称“B专利清单”)。(3)就RPS标出的愿意许可的专利逐一作出回复。
4.RPS反驳
RPS则需在收到上述BA回应的60天内,针对BA的陈述予以详细反驳,包括逐条权利要求地阐述认为所涉生物类似药构成侵权的事实与法律依据,并对BA提出的专利无效、不可执行理由作出回应。
5.确定首轮诉讼的专利范围
在BA收到RPS的反驳后的15天内,双方应协商确定首轮诉讼的涉案专利范围(下称“C专利清单”)。
如果双方无法协商一致,则将启动第二次信息交换:由BA确定首轮诉讼的涉案专利数量并通知RPS。随后双方在5天内同时列出首轮诉讼专利清单,并进行交换,最终确定双方清单上重合的全部专利为首轮诉讼的专利(下称“D专利清单”)。RPS列出的专利数量不能多于BA列出的专利数量;除非BA未列出任何专利,则RPS可列出1项专利。
(二)首轮诉讼阶段
在确定首轮诉讼的专利清单后,RPS应在30天内就清单所列的每一项专利提起侵权诉讼。BA在收到起诉状后的30天内,需通知FDA并提交该起诉状副本。
需注意,如果RPS在向BA提供A专利清单后,又获得新的可能被侵权的专利授权或独占许可,则需要在该新专利获得授权或许可的30天内向BA补充清单,BA则需在收到补充清单的30天内针对补充清单的专利作出回应。补充清单的专利适用于后续的第二轮诉讼阶段。
(三)上市前通知
BA须在其生物类似药首次商业上市前至少180天向RPS发出上市通知。根据最高法院在Sandoz Inc. v. Amgen Inc. 案确认的观点,BA可以选择在其生物类似药的aBLA获得FDA批准上市之前就发出通知,无需等待aBLA获批后。
(四)第二轮诉讼阶段
收到BA的通知后,RPS可发起第二轮的专利诉讼,并可申请禁令阻止相关生物类似药的生产和销售等。第二轮涉案专利须来自专利舞蹈程序早期的专利清单(A专利清单或B专利清单)中,但不能是双方已同意用于首轮诉讼的专利(C专利清单或D专利清单)。
若BA在专利舞蹈程序中按照规定提供了aBLA副本和相关信息,则在BA发出上市通知之前,双方均不得对第二轮诉讼阶段的专利提起确认专利侵权、有效性或可执行性的诉讼。
若BA在专利舞蹈过程中未能遵守相关规则,则RPS有权就A专利清单中的任何专利提起专利侵权诉讼;而BA在提供上市通知之前,不得提起确认专利不侵权、无效或不可执行的确认之诉(Declaratory Judgment)。
深圳知识产权保护中心
2026年3月13日